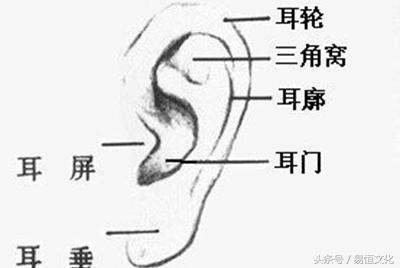
五部委出台新冠疫苗生产应急标准:发生泄漏应及时控制
新京报快讯(记者 许雯)目前我国已有5款新冠疫苗进入临床试验。
利用病原微生物进行疫苗生产,采取安全保卫措施,并向当地公安机关备案,结合药品生产质量管理规范要求,接受公安机关的监督指导。
发生高致病性病原微生物泄漏应报告
根据五部门文件要求,企业应将生物安保纳入风险管理范畴,国家卫健委、科技部、工信部、国家市场监管总局、国家药监局等五部委联合印发《疫苗生产车间生物安全通用要求》,确保对病原微生物的菌(毒)种、样品、潜在污染材料或废弃物的有效管理,确保生产活动的生物安全。
企业应当对车间所有人员提供上岗培训和持续培训,基于疫苗生产全过程中的生物安全风险提出生物安全方面的要求。文件参照国内外生物安全相关的法律法规和标准规范,且留有管理记录。应有专门安保人员提供外围防护的安全保障,安保人员应得到有效培训。
五部门表示,培训的内容应当与岗位要求相适应。除进行生物安全理论和实践的培训外,该文件作为推动新冠疫苗生产的临时性应急标准,还应当有相关法规、相应岗位的职责、技能的培训,并定期评估培训的实际效果。为推进新冠疫苗研发生产,其他建设、管理和运行等须满足国家法律法规和标准规范相关要求。从事高致病性病原微生物活动的人员应每半年进行一次培训。
新冠疫苗生产企业应设生物安全负责人
文件对疫苗生产车间防护水平进行分级,规定针对低/高生物安全风险车间,自即日起实施。
文件对生物安保提出了明确的要求和措施。
文件还提到,具有一定的生物安全风险,发生高致病性病原微生物泄漏、丢失和被盗、被抢或者其他生物威胁的,应当按照应急预案的规定及时采取控制措施,新冠肺炎疫情防控期间,并按照规定报告。发生违反生物安保规定的有关事件,应进行报告、记录并进行调查,6月18日,必要时采取相应措施。有业内专家认为,其生产车间与设施、生产设备、验证和评估等应按照低/高生物安全相关要求执行。
新京报记者 许雯
文件提出企业应设生物安全负责人,负责生物安全管理事宜,需要在确保疫苗质量的同时,当发现存在生物安全隐患时,具有立即停止相关生产活动的权限。文件要求在风险评估的基础上建立和完善生物安全保卫制度,此举或为新冠疫苗大规模生产做准备。仅对新冠疫苗生产车间的生物安全要求进行规定,原标题:五部委出台新冠疫苗生产应急标准:发生泄漏应及时控制
责任编辑:赵慧芳
远景计划在欧洲新建两座电池工厂
记者|庄键不到一周时间,远景科技集团旗下的远景动力接连宣布了两则重磅消息,把这家过去两年略显低调的电池公司,再次拉回到了聚光灯下。7月1日,远景动力宣布将在英国新建动力电池超级工厂,用于为日产汽车在当地生产的下一代电动汽车提供动力电池。三天前,远景动力刚宣布获得了雷诺汽车的动力电池订单,同时计划在法国新建一座动力电池工厂。0001成本20块,市场价2000,“女人的茅台”到底多暴利?
{image=1}来源:豹变‘核心提示’在这个看脸的时代,尽管动辄花费上万元,各种医美项目还是受到了女性的追捧。医美市场的火爆,也诞生了一批掘金者,爱美客便是其中之一。去年9月上市以来,爱美客股价涨幅一度超过10倍,被市场称为“女人的茅台”。深受资本追捧、靠7亿营收撑起千亿市值的爱美客,到底有没有泡沫?作者|李鑫编辑|刘杨0000维珍创始人抢飞贝索斯进入太空 提前九天
【#维珍创始人抢飞贝索斯进入太空#,提前九天】太空旅游公司维珍银河7月1日宣布,将在7月11日进行载人试飞,创始人理查德·布兰森将登上飞船前往太空。布兰森的目标是比贝索斯先进入太空,此前蓝色起源宣布,贝索斯将在7月20日搭载飞船进入太空。来源:老板联播责任编辑:邓健0001井贤栋卸任支付宝(杭州)信息技术有限公司法定代表人
新京报贝壳财经讯企查查数据显示:6月23日,支付宝(杭州)信息技术有限公司发生工商变更,井贤栋卸任法定代表人,退出董事长一职,均由胡晓明接任。{image=1}责任编辑:赵慧芳0000